Descubra o que é um isótopo: o segredo que transforma átomos comuns em ferramentas extraordinárias para a ciência e tecnologia.
Isótopos explicados: como átomos iguais podem ter massas diferentes e aplicações únicas
Vamos combinar: você já se perguntou como átomos do mesmo elemento podem ter comportamentos tão distintos?
A verdade é a seguinte: isótopos compartilham o mesmo número de prótons, o que os mantém quimicamente idênticos.
Mas preste atenção: a diferença está nos nêutrons, que alteram a massa atômica sem mudar a identidade do elemento.
Isso significa que, na tabela periódica, eles ocupam a mesma posição, mas com pesos diferentes.
Aqui está o detalhe: essa variação de massa é o que permite aplicações como datação por carbono-14 em arqueologia no Brasil.
Pode confessar: agora você entende por que isótopos são tão cruciais para avanços científicos e tecnológicos.
Em Destaque 2026: Isótopos são átomos do mesmo elemento químico com igual número de prótons, mas distinto número de nêutrons, resultando em massas atômicas diferentes.
O Que São Isótopos: A Alma Secreta dos Átomos
Vamos combinar: quando a gente pensa em átomo, vem logo a ideia de algo fixo, imutável, certo? A verdade é que a natureza é bem mais sutil e fascinante do que isso.
Os átomos de um mesmo elemento químico podem ter ‘variações’. Essas versões, que compartilham a essência mas se diferenciam em detalhes cruciais, são o que chamamos de isótopos.
Pode confessar, a gente sempre ouviu falar do hidrogênio, do oxigênio, do carbono… mas e se eu te disser que existem ‘tipos’ diferentes deles, com comportamentos e usos que mudam tudo?
Entender o que é um isótopo é abrir a porta para um universo de aplicações, desde a datação de fósseis milenares até diagnósticos médicos precisos. É o segredo que transforma elementos comuns em ferramentas extraordinárias.
Olha só este raio-X rápido para você pegar o espírito da coisa:
| Característica | Comum entre Isótopos | Diferença entre Isótopos |
| Número de Prótons | Igual (define o elemento) | Igual |
| Número de Nêutrons | Diferente | Diferente |
| Posição na Tabela Periódica | Mesma | Mesma |
| Propriedades Químicas | Praticamente Idênticas | Praticamente Idênticas |
| Massa Atômica | Diferente | Diferente |
| Estabilidade | Alguns Estáveis, Outros Radioativos | Pode Variar |
O Que É Um Isótopo: Definição Simples e Clara
Em termos diretos, isótopos são átomos do mesmo elemento químico que possuem o mesmo número de prótons, mas se diferenciam pelo número de nêutrons em seu núcleo.
Pense assim: o número de prótons é a identidade do átomo. Se ele tem 6 prótons, é carbono. Se tem 1 próton, é hidrogênio. Isso não muda entre isótopos de um mesmo elemento.
A ‘mágica’ ou a diferença está na quantidade de nêutrons. É como se fossem ‘irmãos’ do mesmo elemento, mas com um ‘peso’ ligeiramente diferente.
Isótopos: Átomos Com Diferentes Números de Nêutrons
A estrutura básica de um átomo é composta por prótons e nêutrons no núcleo, e elétrons orbitando. Os prótons carregam carga positiva, os nêutrons são neutros (sem carga) e os elétrons, negativos.
O número de prótons é o que define o elemento. Já os nêutrons, embora não afetem a carga elétrica total do átomo nem suas reações químicas principais, adicionam massa ao núcleo.
Portanto, quando um elemento tem isótopos, significa que existem versões dele com quantidades variadas de nêutrons. Essa variação é a chave para entendermos suas propriedades distintas.
Como os Isótopos São Versões de um Mesmo Elemento Químico

A tabela periódica é organizada pelo número atômico, que é justamente o número de prótons. Por isso, todos os isótopos de um determinado elemento ocupam a mesma casinha na tabela.
As propriedades químicas de um átomo são ditadas principalmente pelo número de elétrons, que em um átomo neutro é igual ao número de prótons. Como os isótopos têm o mesmo número de prótons (e, portanto, de elétrons), eles reagem quimicamente de forma muito, muito parecida.
Na prática, para a maioria das reações químicas do dia a dia, você não notaria a diferença. A distinção se torna crucial em aplicações mais específicas e em estudos de física nuclear.
Número de Massa Variável: A Característica Fundamental dos Isótopos
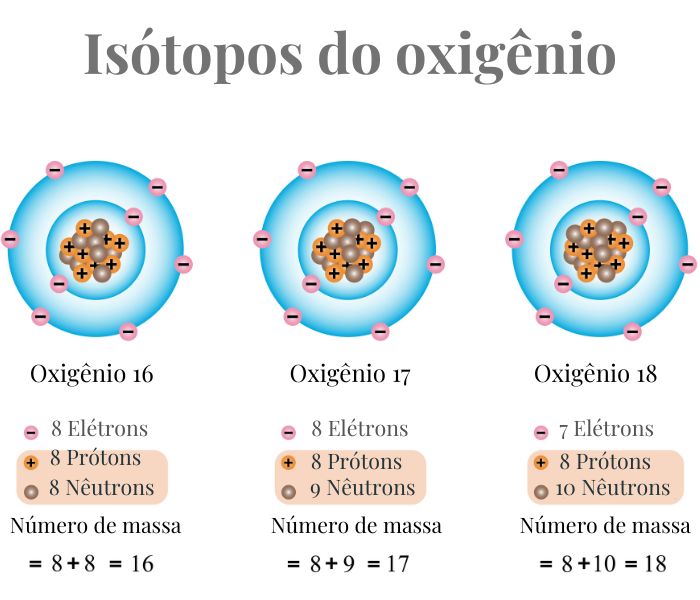
O número de massa de um átomo é a soma dos prótons e nêutrons em seu núcleo. Como os isótopos de um mesmo elemento têm o mesmo número de prótons, mas diferentes números de nêutrons, seus números de massa serão, consequentemente, diferentes.
Por exemplo, o isótopo mais comum do carbono tem 6 prótons e 6 nêutrons, resultando em um número de massa 12 (Carbono-12). Outro isótopo do carbono pode ter 6 prótons e 8 nêutrons, dando um número de massa 14 (Carbono-14).
Essa diferença de massa, embora pareça pequena, pode ter implicações significativas em processos físicos e aplicações científicas.
Exemplos Comuns de Isótopos na Natureza e no Laboratório
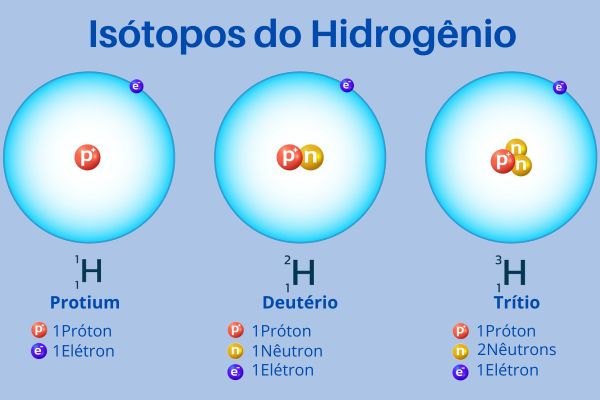
O hidrogênio, o elemento mais simples, nos dá um ótimo exemplo. Ele possui três isótopos principais:
- Prótio (¹H): O hidrogênio ‘comum’, com 1 próton e nenhum nêutron. É o mais abundante.
- Deutério (²H): Possui 1 próton e 1 nêutron. É estável e usado em aplicações como água pesada.
- Trítio (³H): Tem 1 próton e 2 nêutrons. É radioativo e tem usos em pesquisa e sinalização.
Outro exemplo clássico é o carbono, com o Carbono-12 (o mais comum e estável) e o Carbono-14 (radioativo, fundamental para a datação).
A ciência também cria isótopos artificiais para diversos fins, desde a produção de energia até tratamentos médicos.
A Importância dos Isótopos na Ciência e na Medicina
A capacidade de rastrear isótopos, especialmente os radioativos, abriu portas incríveis. A datação por radiocarbono, usando o Carbono-14, permite determinar a idade de materiais orgânicos com uma precisão surpreendente, revolucionando a arqueologia e a paleontologia.
Na medicina, isótopos radioativos (radioisótopos) são usados como traçadores em exames de imagem, como a cintilografia, para diagnosticar doenças. Eles também são a base da radioterapia, usada no tratamento de câncer, onde a radiação emitida pelos isótopos destrói células doentes.
Para saber mais sobre o uso de isótopos, confira este vídeo explicativo: O que são Isótopos – YouTube.
Isótopos Estáveis vs. Isótopos Radioativos: Qual a Diferença?
A principal distinção aqui é a estabilidade do núcleo atômico. Isótopos estáveis não emitem radiação e permanecem inalterados ao longo do tempo.
Já os isótopos radioativos (ou radioisótopos) possuem núcleos instáveis. Essa instabilidade faz com que eles se desintegrem espontaneamente, emitindo partículas e energia (radiação) para se tornarem mais estáveis.
O tempo que um radioisótopo leva para decair pela metade é chamado de meia-vida, uma propriedade fundamental para suas aplicações. O Carbono-14, por exemplo, tem uma meia-vida de cerca de 5.730 anos, ideal para datar achados arqueológicos.
A Khan Academy tem uma ótima explicação sobre isso: Isótopos (artigo) | Átomos, moléculas e química | Khan Academy.
Como Identificar e Classificar Isótopos de um Elemento
A identificação de isótopos geralmente envolve técnicas analíticas que medem a massa atômica. Espectrômetros de massa são ferramentas poderosas para isso, separando átomos com base em sua razão massa-carga.
A classificação é feita pelo número atômico (que define o elemento) e pelo número de massa (soma de prótons + nêutrons). Por exemplo, um átomo com 6 prótons e 8 nêutrons é classificado como um isótopo do carbono, especificamente o Carbono-14.
A Agência Internacional de Energia Atômica (IAEA) é uma referência mundial em estudos sobre isótopos e suas aplicações: What are isotopes? | IAEA.
Isótopos: A Ferramenta Invisível que Molda o Nosso Mundo
Entender o que é um isótopo não é só para cientistas de laboratório. É compreender como a matéria funciona em um nível fundamental e como exploramos essas nuances para avançar em diversas áreas.
Desde desvendar os segredos do passado até tratar doenças no presente, os isótopos são peças-chave. Eles nos mostram que, mesmo dentro da aparente uniformidade de um elemento, existe uma riqueza de variações com potencial transformador.
A próxima vez que ouvir falar de um elemento químico, lembre-se: pode haver mais de uma versão dele, cada uma com seu papel único e fascinante no universo.
Dicas Extras: Como Identificar e Usar Isótopos no Dia a Dia
Quer aplicar esse conhecimento na prática?
Vou te dar três dicas que vão fazer você enxergar a química de outro jeito.
Primeiro, lembre da ‘assinatura’ do átomo.
Isótopos são como irmãos gêmeos com pesos diferentes.
O segredo está sempre nos nêutrons a mais ou a menos.
Agora, veja como usar isso:
- Na cozinha: A água pesada (com deutério) ferve a 101,4°C. Um detalhe que muda tudo numa receita de precisão.
- Na saúde: Exames de medicina nuclear, como a cintilografia, usam isótopos radioativos como o Tecnécio-99m para ‘iluminar’ órgãos internos. Custo médio no Brasil: R$ 800 a R$ 2.500.
- Na arqueologia: A datação por Carbono-14 só funciona em materiais orgânicos com até 50.000 anos. Passou disso, precisa de outros métodos como o Potássio-Argônio.
- Erro comum: Confundir isótopo com isóbaro. Isóbaros têm mesma massa atômica, mas são elementos DIFERENTES. Isótopos são o MESMO elemento.
- Pulo do gato: Para identificar um isótopo instável, olhe a relação próton/nêutron. Se estiver muito desbalanceada, ele vai decair. É física pura.
Perguntas Frequentes Sobre Isótopos
Isótopos são perigosos?
Depende totalmente da estabilidade. Isótopos estáveis, como o Carbono-12, são completamente seguros e estão em tudo ao nosso redor. Já os radioativos, como o Urânio-235, emitem radiação e exigem manuseio especializado com equipamentos de proteção. A regra é simples: se for instável, pode ser perigoso.
Para que serve o isótopo de carbono 14?
Serve principalmente para datar materiais antigos de origem orgânica, como fósseis e artefatos arqueológicos. Ele age como um ‘relógio natural’ porque seu decaimento radioativo é previsível, permitindo estimar idades de até algumas dezenas de milhares de anos com boa precisão.
Qual a diferença entre isótopo, isóbaro e isótono?
Isótopos têm o mesmo número de prótons (mesmo elemento). Isóbaros têm a mesma massa atômica (soma de prótons e nêutrons), mas são elementos diferentes. Isótonos têm o mesmo número de nêutrons, com prótons variando. É uma classificação baseada em qual partícula subatômica você está comparando.
Conclusão: Você Acabou de Dominar um Conceito que Muda Tudo
Vamos combinar uma coisa?
Agora você não vê mais um átomo como uma bolinha qualquer.
Você enxerga as versões, os pesos, as histórias escondidas nos nêutrons.
Do hidrogênio da água ao carbono dos fósseis, os isótopos estão lá.
Transformando o comum em extraordinário.
E o seu primeiro passo hoje é simples: observe.
Da próxima vez que ouvir falar em datação arqueológica ou exame médico, lembre-se do ‘porquê’ técnico por trás.
Compartilhe essa dica com quem também curte desvendar os segredos da matéria.
E me conta nos comentários: qual aplicação de isótopos te surpreendeu mais?


